|
||
|
|
||
| Главная ≫ Инфотека ≫ Физика ≫ Видео ≫ Люминесценция // Валентина Уточникова |
ЛюминесценцияВалентина Уточникова
Химик Валентина Уточникова о влиянии спектроскопии на развитие люминесценции, создании светодиодов и флуоресценции. Люминесценция — это одно из самых красивых явлений. Оно относится к тем явлениям, которые человечество наблюдает уже очень много лет, хотя объяснять научилось совсем недавно. К люминесценции относится северное сияние, свечение светлячков, свечение морской воды относится к люминесценции проживающего там планктона. И все эти явления человечество наблюдает практически все время своего существования. Первое описание люминесценции возникло примерно в XVII веке одновременно с открытием фосфора. Фосфор (его название так и переводится — «дающий свет») обладает люминесценцией, которая проявляется в результате его окисления. Относится это, конечно, только к белому фосфору. Вы помните собаку Баскервилей, которая ужасная тварь, которая среди ночи пугала посетителей болот, из-за того что морда ее якобы была намазана белым фосфором. На самом деле, конечно, собака, измазанная белым фосфором, не протянула бы долго: мало того, что он просто ядовит, так еще и люминесцирует за счет того, что окисляется, фактически горит. Но тем не менее это один из примеров хемилюминесценции, то есть люминесценции, происходящей за счет энергии, выделяющейся в результате химической реакции. И это первый пример люминесцентного процесса, который был изучен, назван и описан. Впоследствии было проведено наблюдение еще ряда люминесцентных явлений. Это опять же была хемилюминесценция, потому что оказалось, что в ходе довольно многих реакций — в первую очередь это реакция окисления — выделяется свет. И уже ближе к нашему времени, в конце XIX века, люминесценция получила гораздо большее развитие, были описаны другие процессы люминесценции. То есть люминесценция возбуждаема не только химическими реакциями, но существует и катодолюминесценция, триболюминесценция, возникающая при трении, и собственно фотолюминесценция, которая сейчас больше всего известна и лучше изучена, но далеко не первая привлекла внимание человечества. Более широкое распространение люминесценции связано, конечно, с тем, что ей наконец нашли применение. Впервые за долгие годы Стокс в конце XIX века предложил использовать люминесценцию в аналитических целях: для анализа присутствия различных органических соединений по изменению спектра люминесценции, интенсивности и так далее. Но развитие такой аналитический метод получил только в середине XX века в связи с работами советского физика Вавилова. Он написал книгу, которая посвящена этому методу анализа. Оказалось, что люминесцентная спектроскопия как аналитический метод обладает чрезвычайно низким пределом обнаружения. Это его огромное достоинство, которое выделяет его на фоне множества других аналитических методов. Развитие этого аналитического метода привело к развитию люминесценции в целом. В Советском Союзе появилась школа, связанная с изучением люминесценции. Естественно, этот процесс развивался и по всему миру. Нам приятно просто вспомнить Вавилова, а вообще говоря, во всем мире происходило изучение люминесценции. Тогда же были введены основные понятия, количественно характеризующие люминесценцию, существенно расширился круг изучаемых люминесцентных материалов. Середину XX века можно считать моментом зарождения люминесценции как науки. Использование люминесценции как аналитического метода до сих пор происходит. Но сейчас развитие этой науки направлено скорее на создание новых люминесцентных материалов. Самое время, прежде чем перейти к описанию этих материалов, дать определение люминесценции. Сам Вавилов в свое время назвал люминесценцию избытком над тепловым излучением тела, длительность которого превышает 10-10 секунды. Это определение, несмотря на то что не дает никакого понятия о том, как искать люминесцентные материалы, довольно точно люминесценцию характеризует, поскольку позволяет отсечь ее от других процессов излучения света. В частности, это избыток нетеплового излучения. То есть самое известное нам излучение — солнечный свет — не относится к люминесценции, поскольку является излучением абсолютно черного тела. Кроме того, есть отражение, рассеяние, комбинационное рассеяние — все эти процессы обладают длительностью меньше 10-10 и тоже люминесценцией не являются. Все остальное таким методом отрицания мы можем отнести к люминесценции. Если рассматривать, откуда берется люминесценция (а важно это понимать, для того чтобы создавать люминесцентные материалы), то люминесценция представляет собой свет, который выделяется за счет энергии, выделяемой во время перехода соединения из возбужденного состояния в основное. Значит, у нас есть соединение, оно может быть органическим или неорганическим, состояние с наименьшей энергией — это основное состояние. Если мы каким-то образом переводим соединение в возбужденное состояние, то есть обладающее большей энергией, то дальше оно может вернуться в основное состояние любым доступным ему способом, но в том числе выделяя энергию, которая расходуется на образование фотонов, квантов света. Если это счастливое событие происходит, то мы говорим о люминесценции. Важно в данном случае, во-первых, привести соединение в возбужденное состояние, во-вторых, обеспечить его возврат в основное состояние с выделением квантов света, наиболее эффективно избегая конкурирующих процессов. Например, энергию можно потратить на тепло, на колебания, в том числе на химические реакции, которые тоже могут протекать. Если мы счастливо этого избегаем, мы имеем эффективно люминесцирующий материал. Среди основных люминесцентных материалов, которые используются на сегодняшний день и развиваются в дальнейшем для их практического использования, можно выделить органические соединения, в том числе металлорганические и координационные. И можно выделить неорганические соединения, к которым следует отнести квантовые точки. Органические соединения также называют органическими красителями, поскольку большинство из них окрашены. Если переход из возбужденного состояния в основное сопровождается выделением кванта света в видимом диапазоне, то логично ожидать, что из основного в возбужденное (а это и есть поглощение) переход тоже происходит поглощением видимого света. Вещество, таким образом, скорее всего, будет окрашено. Органические люминесцирующие соединения — это в основном сопряженные соединения, ароматические либо сопряженные полимеры. Изменяя степень сопряжения, вводя те или иные заместители, мы можем изменять энергию возбужденного состояния и длину волны люминесценции от видимого синего до красного и даже невидимого, ультрафиолетового или ультракрасного излучения. Это сейчас одна из довольно важных задач, особенно получение инфракрасной люминесценции. Введение в состав органического соединения металла с образованием координационного соединения или металлорганического соединения приводит к изменению люминесцентных характеристик. Либо это будет просто изменение спектра, ширины полосы, эффективности люминесценции. Кроме того, введение тяжелого металла может приводить к изменению самого характера люминесценции, к замене флуоресценции на фосфоресценцию. В соответствии с определением, принятым уже на сегодняшний день, флуоресценция — это быстрая люминесценция. Она происходит без изменения спина. Возбужденное и основное состояние у нас имеет одну и ту же мультиплетность. Если люминесценция происходит из возбужденного состояния одной мультиплетности в основное состояние другой мультиплетности, мы имеем запрещенный переход, длительность его будет большой, и это фосфоресценция. Введение тяжелого металла — иридия или платины — в состав соединения с образованием металлорганического соединения приводит к тому, что запрет на этот переход частично снимается и соединение способно к фосфоресценции. Это очень важно для создания органических светодиодов. Есть и неорганические соединения, обладающие люминесценцией. Это полупроводниковые соединения, поскольку для люминесценции, для перехода из возбужденного состояния в основное, нам нужно, чтобы был зазор между этими состояниями. В терминах физики полупроводников это зазор между дном зоны проводимости и потолком валентной зоны полупроводника. Переход из такого возбужденного состояния в основное тоже может сопровождаться выделением света. На этом основано получение неорганических люминофоров, в частности, для создания неорганических светодиодов. Квантовые точки представляют собой очень интересный класс материалов, поскольку в данном случае этот зазор между возбужденным и основным состоянием образуется за счет так называемого эффекта электрона в квантовой яме. Если полупроводник ограничить по размеру, получить какой-то нанокристалл или одномерный кристалл (это плоскость, ограниченная в одном направлении), двумерный кристалл (какую-то протяженную структуру) или ограничить в трех направлениях, то мы получаем задачу об электроне в квантовой яме, решением которой является набор дискретных уровней, разница по энергии между которыми зависит от размера этой ямы — от размера наночастицы. Таким образом, используя один и тот же материал, но получая его в виде наночастиц разного размера, мы можем получить люминофор, излучающий разный свет — от синего до красного, даже ультрафиолетовый или инфракрасный. И отдельным классом соединений являются соединения лантанидов. Ионы лантанидов — это f-элементы. У них есть f-орбитали, частично заполненные электронами. И перераспределение этих электронов по f-орбиталям приводит к образованию различных возбужденных состояний. Разница по энергии между этими состояниями также лежит в ультрафиолетовой, видимой и инфракрасной областях, и эти соединения тоже потенциально способны к люминесценции. На их основе получают как неорганические, так и координационные соединения. Особенностью этих соединений является то, что люминесценция в них является запрещенным процессом, поэтому характеризуется чрезвычайно большим временем жизни возбужденного состояния, происходит очень медленно. Это позволяет создавать на основе неорганических соединений, допированных лантанидами, лазеры. Один из самых известных — это неодимовый лазер. А кроме того, можно использовать их в медицине, где тоже важно большое время жизни возбужденного состояния. Поскольку переход запрещенный, то и поглощение тоже малоинтенсивно. Для того чтобы обойти этот запрет, используют координационные соединения лантанидов, где поглощение обеспечивается органическим лигандом. И при правильном подборе органического лиганда он может быть использован как антенна, эффективно передающая излучение с органического лиганда на ион, который затем и люминесцирует. Все эти классы соединений имеют свои применения на сегодняшний день: это и лазеры, которые я уже упоминала, и аналитика, и медицинская диагностика, и органические светодиоды, которые используются, например, в экранах мобильных телефонов. Но вариантов развития для них еще больше. Это может быть люминесцентный термометр, например, up-конверсионные материалы, которые переизлучают инфракрасный свет в видимый. И их дальнейшее развитие является предметом изучения ученых по всему миру сегодня. Валентина Уточникова, кандидат химических наук, МГУ им. М.В. Ломоносова ПостНаука
ТегиПохожее
|
| Главная ≫ Инфотека ≫ Физика ≫ Видео ≫ Люминесценция // Валентина Уточникова |
|
[time: 14 ms; queries: 7]
31 Мая 2026 16:56:03 GMT+3 |


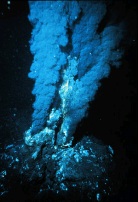 Химики показали, что в гидротермальных источниках при температуре свыше 80 градусов может происходить абиогенный синтез органических веществ, в частности аминокислот, из угарного газа, цианистого водорода и других неорганических соединений. Это открытие — важный аргумент в пользу гипотезы, согласно которой жизнь на Земле зародилась в горячих вулканических источниках.
Химики показали, что в гидротермальных источниках при температуре свыше 80 градусов может происходить абиогенный синтез органических веществ, в частности аминокислот, из угарного газа, цианистого водорода и других неорганических соединений. Это открытие — важный аргумент в пользу гипотезы, согласно которой жизнь на Земле зародилась в горячих вулканических источниках. Самый редкий элемент в земной коре, самым тяжелый газ, самый тугоплавкий материал, самый сильный стабильный окислитель, самая сильная кислота, самый сильный яд, самое сладкое вещество — и другие рекорды.
Самый редкий элемент в земной коре, самым тяжелый газ, самый тугоплавкий материал, самый сильный стабильный окислитель, самая сильная кислота, самый сильный яд, самое сладкое вещество — и другие рекорды. Взрывная история химии — это история строительных блоков, которые составляют весь наш мир, история химических элементов. Все в мире состоит из элементов — земля по которой мы ходим, воздух которым мы дышим, даже мы сами. Несмотря на это, на протяжении веков этот мир понимался совершенно неправильно. В трехсерийном фильме профессор теоретической физики Джим Аль-Халили проследит удивительную историю о том, как элементы были обнаружены и сведены в таблицу. Он пройдет по следам первопроходцев, раскрывших эти секреты и создавших новую науку, которая привела нас к эпохе современности.
Взрывная история химии — это история строительных блоков, которые составляют весь наш мир, история химических элементов. Все в мире состоит из элементов — земля по которой мы ходим, воздух которым мы дышим, даже мы сами. Несмотря на это, на протяжении веков этот мир понимался совершенно неправильно. В трехсерийном фильме профессор теоретической физики Джим Аль-Халили проследит удивительную историю о том, как элементы были обнаружены и сведены в таблицу. Он пройдет по следам первопроходцев, раскрывших эти секреты и создавших новую науку, которая привела нас к эпохе современности. Известная из школьного курса химия говорит преимущественно о том, что случается при «нормальных условиях». Принципиальное изменение этих условий может вести к изменению не только физических, но и химических свойств, что помогает создавать принципиально новые материалы.
Известная из школьного курса химия говорит преимущественно о том, что случается при «нормальных условиях». Принципиальное изменение этих условий может вести к изменению не только физических, но и химических свойств, что помогает создавать принципиально новые материалы. Лекции доктора физико-математических наук, ведущего научного сотрудника сектора математической физики Физического Института им. П.Н. Лебедева РАН, Москва; Directeur de Recherche au CNRS (CNRS — Национальный центр научных исследований) Universite Paris-Sud, Орсэ, Франция Сергея Нечаева, прочитанной 11 апреля 2012 года в рамках проекта «Публичные лекции "Полит.ру"»
Лекции доктора физико-математических наук, ведущего научного сотрудника сектора математической физики Физического Института им. П.Н. Лебедева РАН, Москва; Directeur de Recherche au CNRS (CNRS — Национальный центр научных исследований) Universite Paris-Sud, Орсэ, Франция Сергея Нечаева, прочитанной 11 апреля 2012 года в рамках проекта «Публичные лекции "Полит.ру"» Беседа с доктором физико-математических наук, ведущим научным сотрудником сектора математической физики ФИАН; Directeur de Recherche au CNRS (CNRS — Национальный центр научных исследований) Universite Paris-Sud, Орсэ (Франция) Сергеем Нечаевым посвящена теме предстоящей лекции о топологии веревок, неевклидовой геометрии и фрактальной укладке ДНК в хромосомах.
Беседа с доктором физико-математических наук, ведущим научным сотрудником сектора математической физики ФИАН; Directeur de Recherche au CNRS (CNRS — Национальный центр научных исследований) Universite Paris-Sud, Орсэ (Франция) Сергеем Нечаевым посвящена теме предстоящей лекции о топологии веревок, неевклидовой геометрии и фрактальной укладке ДНК в хромосомах. Вместе с профессором Маркусом дю Сотоем мы отправимся в удивительное путешествие в мир измерений. Он попытается узнать, почему мы постоянно хотим измерить и определить количество всего, что нас окружает. Мы узнаем, как были определены такие понятия как метр, секунда и величина веса, а также как мы научились измерять высокие температуры, свет и электричество.
Вместе с профессором Маркусом дю Сотоем мы отправимся в удивительное путешествие в мир измерений. Он попытается узнать, почему мы постоянно хотим измерить и определить количество всего, что нас окружает. Мы узнаем, как были определены такие понятия как метр, секунда и величина веса, а также как мы научились измерять высокие температуры, свет и электричество.