|
||
|
|
||
| Главная ≫ Инфотека ≫ Химия ≫ Элементы жизни: почему не кремний и не фтор / Биогенез // Михаил Никитин |
Элементы жизни: почему не кремний и не фтор / БиогенезМихаил Никитин
Элементы жизни: почему не кремний и не фторНикитин М.А. 
Почему все живое состоит из углерода, кислорода, азота и водорода? Стандартный ответ, который можно найти в литературе: потому, что атомы углерода способны образовывать цепочки и кольца, создавая гигантское разнообразие органических молекул. И потому, что вода — вещество с уникальными свойствами, способное растворять огромное разнообразие веществ, а также стабилизировать температуру за счет высокой теплоемкости, теплоты замерзания и теплоты испарения Экзобиологические исследования (поиски жизни вне Земли) концентрируются на планетах с такой температурой поверхности, при которой возможно существование жидкой воды. Великий астроном Карл Саган жестко критиковал эту позицию, называя ее «водно-углеродным шовинизмом». По его мнению, другим ученым просто не хватает фантазии, чтобы представить себе альтернативную биохимию на иных химических элементах В фантастике часто можно встретить описания кремнийорганической жизни или жизни, использующей фтороводород либо аммиак в качестве растворителя. Кремний действительно способен образовывать сложные молекулы с длинными цепочками и кольцами атомов. Такой же способностью обладает и бор, на который, насколько мне известно, фантасты не обращали внимания. Воду в качестве растворителя действительно могут заменить NH3 и HF. Однако я придерживаюсь водно-углеродного шовинизма и собираюсь обосновать свою позицию при помощи ядерной физики. Во Вселенной больше всего водорода, второе место за гелием (рис. 1). Следом идут углерод, кислород и азот. Три легких элемента — литий, бериллий, бор — весьма редки. От кислорода и до титана распространенность элементов плавно убывает, причем элементы с нечетными атомными номерами встречаются реже, чем с четными. Затем идут несколько широко распространенных металлов — хром, марганец, железо, никель. Элементы, следующие за никелем и особенно за цинком, совсем редки.
Почему так получается? Ядра тяжелее дейтерия (тяжелого водорода) образуются в основном в термоядерных реакциях, протекающих в звездах. Простейшая из таких реакций, имеющая самую низкую температуру зажигания, — протон-протонный цикл. Благодаря ему светят Солнце и другие звезды небольшой массы. В этой реакции четыре протона в несколько стадий превращаются в ядро гелия с выделением энергии (D — дейтерий, e+ — позитрон, νe — электронное нейтрино, γ — фотон): p + p → ²D + e+ + νe + 0,4 МэВ, ²D + p → 3He + γ + 5,49 МэВ, 3He + 3He → 4He + 2p + 12,85 МэВ. В более массивных звездах (от полутора масс Солнца) зажигается следующая реакция — углерод-азотный цикл. В нем также протоны превращаются в ядра гелия, а ядро углерода выступает в качестве катализатора Второй итог этой реакции — частичное превращение углерода в азот и кислород: 12C + p → 13N + γ + 1,95 МэВ, 13N → 13C + e+ + νe + 1,37 МэВ, 13C + p → 14N + γ + 7,54 МэВ, 14N + p → 15O + γ +7,29 МэВ, 15O → 15N + e+ + νe + 2,76 МэВ, 15N + p → 12C + 4He + 4,96 МэВ. Так или иначе, со временем в центре звезды кончается водород и образуется скопление гелия. Горение водорода продолжается в тонком слое вокруг гелиевого ядра. Внешние оболочки звезды при этом раздуваются, звезда становится красным гигантом Если масса звезды невелика, то по мере исчерпания водорода в центре оболочка будет сброшена, а горячая гелиевая сердцевина станет видна на небе как белый карлик и за несколько миллионов лет остынет и погаснет. Жизнь тяжелых звезд оказывается интереснее. Их гелиевая сердцевина разогревается настолько, что в ней зажигается следующая термоядерная реакция — 3-альфа-процесс, превращение гелия в углерод: 4He + 4He → 8Be + γ + 0,09 МэВ, 8Be + 4He → 12C + γ + 7,37 МэВ. Стареющая звезда получает новый мощный источник энергии и становится сверхгигантом. У более массивных сверхгигантов по мере сгорания гелия начинаются термоядерные реакции с участием углерода и кислорода, в них образуются ядра неона, магния, кремния, серы и так далее — изотопы с четным числом протонов и нейтронов: 12C + 12C → 20Ne + 4He, 12C + 16O → 24Mg + 4He, 16O + 16O → 28Si + 4He, 16C + 20Ne → 32S + 4He. Выделяющиеся альфа-частицы также могут захватываться ядрами: 20Ne + 4He → 24Mg + γ, 24Mg + 4He → 28Si + γ, 28Si + 4He → 32S + γ. Чем более тяжелые ядра сливаются, тем быстрее идут реакции. Если горение водорода в массивной звезде растягивается на десятки миллионов лет, то горение гелия продолжается только сотни тысяч лет. Горение углерода и кислорода с образованием неона, магния и кремния занимает сотни лет. Наконец, превращение кремния и серы в металлы занимает сутки. Выделение энергии в этих реакциях заканчивается с образованием ядер 56Ni и 60Zn, синтез более тяжелых ядер происходит уже с поглощением энергии. В центре звезды-сверхгиганта накапливаются металлы, и выделение энергии прекращается. Остывание центра звезды приводит к потере устойчивости — оболочки начинают падать к центру, звезда сжимается и взрывается. Светимость звезды в этот момент возрастает в миллиарды раз, и астрономы говорят о вспышке сверхновой. В нижних слоях ядра образуется огромное количество нейтронов, которые быстро захватываются атомными ядрами. Так синтезируются все возможные тяжелые элементы от натрия и магния до нестабильных трансурановых, как четные, так и нечетные. Ударная волна разносит все оболочки звезды по космосу, первые тысячи лет после этого они видны как светящаяся планетарная туманность. На месте звезды остается маленький сверхплотный остаток — нейтронная звезда или черная дыра, а большая часть вещества возвращается в газопылевые облака, обогащая их тяжелыми элементами. Есть несколько типов ядер, которые синтезируются в других процессах. Во-первых, это дейтерий — тяжелый водород. В звездах он быстро превращается в гелий, и считается, что современные запасы дейтерия образовались из водорода вскоре после Большого взрыва, причем от превращения в гелий их предохранило быстрое остывание Вселенной. Во-вторых, три легких элемента — литий, бериллий и бор — в условиях звезд легко превращаются в гелий и углерод, и их синтез происходит в межзвездной среде в реакциях с участием космических лучей. Пики на графике, соответствующие свинцу, урану и торию, означают, что заметная часть этих элементов образовалась путем распада их более тяжелых соседей. Свинец и висмут — два последних стабильных элемента, а уран и торий — два последних относительно стабильных (период полураспада измеряется миллиардами лет). Таким образом, существование жизни на основе бора запрещено ядерной физикой: малая устойчивость ядра этого элемента приводит к тому, что его содержание во Вселенной в миллион раз меньше, чем кислорода и углерода. Об этом можно сожалеть, потому что химия бора интересна и разнообразна, а в паре с азотом он может образовать близкие аналоги органических соединений углерода (рис. 2):
С кремниевой жизнью сложнее. Хотя сам кремний доступен в изобилии, в присутствии кислорода и воды он склонен образовывать весьма устойчивые нерастворимые силикаты. В отличие от углерода, кремний не образует сложные пи-связи, охватывающие более двух атомов, — а только благодаря пи-связям органические молекулы способны к сложным взаимодействиям со светом, вплоть до фотосинтеза (рис. 3).
Синтез большинства кремнийорганических веществ требует отсутствия воды. Более подходящим растворителем был бы фтороводород HF. Однако единственный устойчивый изотоп фтора — 19F — образуется в звездных ядерных реакциях с весьма малым выходом, и содержание фтора во Вселенной примерно в десять тысяч раз ниже, чем кислорода. Кислород же и углерод являются самыми распространенными элементами Вселенной после водорода и гелия, и неудивительно, что живые организмы состоят в основном из них. Пока остановимся на этом, а в следующем номере расскажем, как возникли первые научные представления о происхождении жизни.
ТегиПохожее
|
| Главная ≫ Инфотека ≫ Химия ≫ Элементы жизни: почему не кремний и не фтор / Биогенез // Михаил Никитин |
|
[time: 9 ms; queries: 8]
2 Мая 2026 13:59:06 GMT+3 |


 Химики показали, что в гидротермальных источниках при температуре свыше 80 градусов может происходить абиогенный синтез органических веществ, в частности аминокислот, из угарного газа, цианистого водорода и других неорганических соединений. Это открытие — важный аргумент в пользу гипотезы, согласно которой жизнь на Земле зародилась в горячих вулканических источниках.
Химики показали, что в гидротермальных источниках при температуре свыше 80 градусов может происходить абиогенный синтез органических веществ, в частности аминокислот, из угарного газа, цианистого водорода и других неорганических соединений. Это открытие — важный аргумент в пользу гипотезы, согласно которой жизнь на Земле зародилась в горячих вулканических источниках. Эта книга предназначена для широкого круга читателей, желающих узнать больше об окружающем нас мире и о самих себе. Автор, известный ученый и популяризатор науки, с необычайной ясностью и глубиной объясняет устройство Вселенной, тайны квантового мира и генетики, эволюцию жизни и показывает важность математики для познания всей природы и человеческого разума в частности.
Эта книга предназначена для широкого круга читателей, желающих узнать больше об окружающем нас мире и о самих себе. Автор, известный ученый и популяризатор науки, с необычайной ясностью и глубиной объясняет устройство Вселенной, тайны квантового мира и генетики, эволюцию жизни и показывает важность математики для познания всей природы и человеческого разума в частности.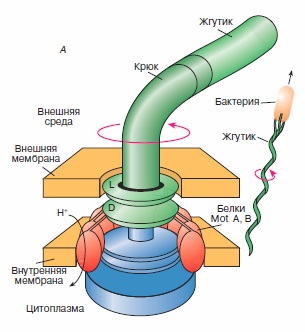 Рассмотрены строение и механизмы действия протонной АТРсинтазы и флагеллярного мотора - молекулярных моторов живой клетки, выполняющих химическую и механическую работу, связанную с их вращательным движением, строение и механизмы работы миозина и кинезина - механохимических белков, ответственных за сократительную активность и внутриклеточный транспорт органелл в клетке.
Рассмотрены строение и механизмы действия протонной АТРсинтазы и флагеллярного мотора - молекулярных моторов живой клетки, выполняющих химическую и механическую работу, связанную с их вращательным движением, строение и механизмы работы миозина и кинезина - механохимических белков, ответственных за сократительную активность и внутриклеточный транспорт органелл в клетке.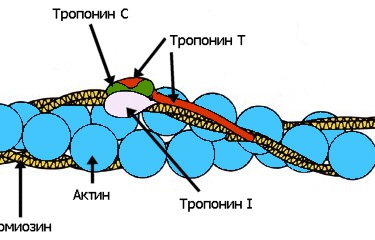 Почти всякая незыблемая общепринятая теория, которую с проклятьями зубрят школьники и которую устало и одинаково рассказывают учителя и даже профессора ВУЗов, при внимательном рассмотрении оказывается отнюдь не однозначной, захватывающей и полной загадок. К теории мышечного сокращения вышесказанное относится в полной мере. В общих чертах она была разработана еще в 50-х годах прошлого века, и классический рисунок с актиновыми и миозиновыми нитями до сих пор кочует из учебника в учебник. Однако реальная картина сокращения мышцы куда запутаннее, интереснее и непонятнее, со множеством подробностей и неожиданных действующих лиц и со сложными ролями, которые исполняют эти лица.
Почти всякая незыблемая общепринятая теория, которую с проклятьями зубрят школьники и которую устало и одинаково рассказывают учителя и даже профессора ВУЗов, при внимательном рассмотрении оказывается отнюдь не однозначной, захватывающей и полной загадок. К теории мышечного сокращения вышесказанное относится в полной мере. В общих чертах она была разработана еще в 50-х годах прошлого века, и классический рисунок с актиновыми и миозиновыми нитями до сих пор кочует из учебника в учебник. Однако реальная картина сокращения мышцы куда запутаннее, интереснее и непонятнее, со множеством подробностей и неожиданных действующих лиц и со сложными ролями, которые исполняют эти лица. Запах корицы и яблок — бабушкин пирог, запах хвои и мандаринов — Новый год, сладкий дурман черемухи — весна… Каждый человек сможет добавить к этому списку длинный ряд своих собственных ассоциаций. Многообразие растительных ароматов, созданных природой, кажется неисчерпаемым, многие из них абсолютно уникальны. Для обозначения таких веществ, которые не принимают непосредственного участия в росте, развитии и репродукции отдельных клеток, более 200 лет назад был предложен термин «вторичные метаболиты». Несмотря на несколько неуважительное название, вещества эти выполняют важную роль в жизни растения в целом, участвуют во взаимодействии растений друг с другом и с окружающей средой. К настоящему моменту идентифицировано более 100000 таких веществ, многие из которых являются легколетучими, и люди воспринимают их как запах растения. В этой лекции я постараюсь рассказать о некоторых особенностях пахучих растений, немного о том, как изучают биосинтез летучих вторичных метаболитов, а также о перспективах применения этих знаний на практике…
Запах корицы и яблок — бабушкин пирог, запах хвои и мандаринов — Новый год, сладкий дурман черемухи — весна… Каждый человек сможет добавить к этому списку длинный ряд своих собственных ассоциаций. Многообразие растительных ароматов, созданных природой, кажется неисчерпаемым, многие из них абсолютно уникальны. Для обозначения таких веществ, которые не принимают непосредственного участия в росте, развитии и репродукции отдельных клеток, более 200 лет назад был предложен термин «вторичные метаболиты». Несмотря на несколько неуважительное название, вещества эти выполняют важную роль в жизни растения в целом, участвуют во взаимодействии растений друг с другом и с окружающей средой. К настоящему моменту идентифицировано более 100000 таких веществ, многие из которых являются легколетучими, и люди воспринимают их как запах растения. В этой лекции я постараюсь рассказать о некоторых особенностях пахучих растений, немного о том, как изучают биосинтез летучих вторичных метаболитов, а также о перспективах применения этих знаний на практике…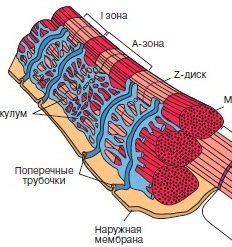 В основе сокращения мышц лежит взаимное перемещение двух систем нитей, образованных актином и миозином. АТФ гидролизуется в активном центре, расположенном в головках миозина. Гидролиз сопровождается изменением ориентации головок миозина и перемещением нитей актина. Регуляция сокращения обеспечивается специальными Са-связывающими белками, расположенными на нитях актина или миозина.
В основе сокращения мышц лежит взаимное перемещение двух систем нитей, образованных актином и миозином. АТФ гидролизуется в активном центре, расположенном в головках миозина. Гидролиз сопровождается изменением ориентации головок миозина и перемещением нитей актина. Регуляция сокращения обеспечивается специальными Са-связывающими белками, расположенными на нитях актина или миозина. Какого цвета могут быть внеземные растения? С научной точки зрения это отнюдь не праздный вопрос, так как цвет поверхности планеты может указать нам, есть ли на ней жизнь, а точнее — живые организмы, усваивающие энергию света своей звезды путем фотосинтеза.
Какого цвета могут быть внеземные растения? С научной точки зрения это отнюдь не праздный вопрос, так как цвет поверхности планеты может указать нам, есть ли на ней жизнь, а точнее — живые организмы, усваивающие энергию света своей звезды путем фотосинтеза. Лекции доктора физико-математических наук, ведущего научного сотрудника сектора математической физики Физического Института им. П.Н. Лебедева РАН, Москва; Directeur de Recherche au CNRS (CNRS — Национальный центр научных исследований) Universite Paris-Sud, Орсэ, Франция Сергея Нечаева, прочитанной 11 апреля 2012 года в рамках проекта «Публичные лекции "Полит.ру"»
Лекции доктора физико-математических наук, ведущего научного сотрудника сектора математической физики Физического Института им. П.Н. Лебедева РАН, Москва; Directeur de Recherche au CNRS (CNRS — Национальный центр научных исследований) Universite Paris-Sud, Орсэ, Франция Сергея Нечаева, прочитанной 11 апреля 2012 года в рамках проекта «Публичные лекции "Полит.ру"»