|
||
|
|
||
| Главная ≫ Инфотека ≫ Биология ≫ Как и почему мышцы сокращаются? Новая модель мышечного сокращения «Поворот и замок» |
Как и почему мышцы сокращаются? Новая модель мышечного сокращения «Поворот и замок»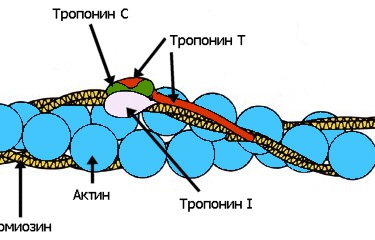
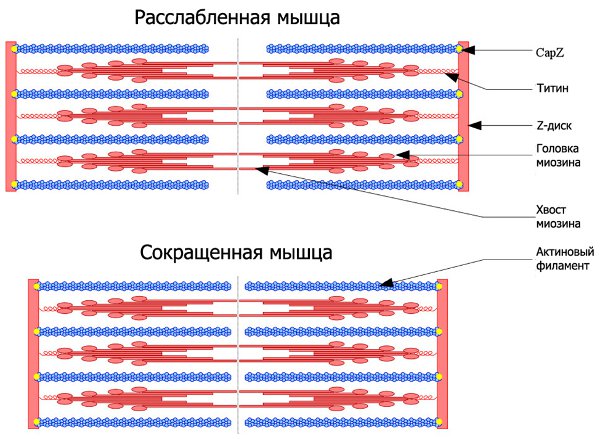
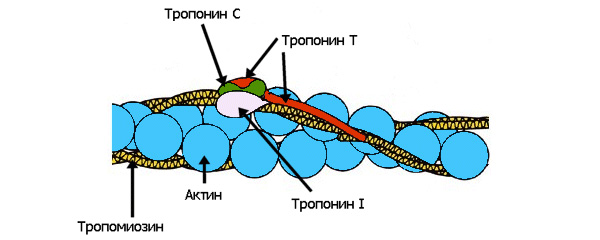
Почти всякая незыблемая общепринятая теория, которую с проклятьями зубрят школьники и которую устало и одинаково рассказывают учителя и даже профессора ВУЗов, при внимательном рассмотрении оказывается отнюдь не однозначной, захватывающей и полной загадок. К теории мышечного сокращения вышесказанное относится в полной мере. В общих чертах она была разработана еще в 50-х годах прошлого века, и классический рисунок (рис. 1) с актиновыми и миозиновыми нитями до сих пор кочует из учебника в учебник. Однако реальная картина сокращения мышцы куда запутаннее, интереснее и непонятнее, со множеством подробностей и неожиданных действующих лиц и со сложными ролями, которые исполняют эти лица. О новой и удивительной отрасли науки, находящейся на стыке физики, математики и биологии и изучающей механизмы мышечного сокращения, рассказали в своих лекциях на проходящей при поддержке РВК, Фонда «Династия» и РФФИ Зимней школе Future Biotech доктор физико-математических наук Андрей Кимович Цатурян и доктор биологических наук, заведующий Лабораторией биологической подвижности Института иммунологии и физиологии УрО РАН Сергей Юрьевич Бершицкий. Азбучные истиныНачнем с азов — собственно, с классической теории мышечного сокращения. Базовая сократительная единица мышечной ткани называется саркомером. Края саркомера — Z-диски — состоят из переплетающихся нитей различных белков. К одному из этих белков цепляются актиновые микрофиламенты, вдоль которых тянутся регуляторные белки тропонин и тропомиозин (рис. 2). Другой белок — титин, самый большой из известных в настоящее время белков, — крепится к соседнему участку Z-диска и служит длинной-длинной основой, с которой связываются молекулы белка миозина. Таким образом, саркомер состоит из чередующихся тонких (образованных многочисленными молекулами актина и регуляторными белками) и толстых (состоящих из тоже многочисленных молекул миозина и вспомогательных белков) нитей.
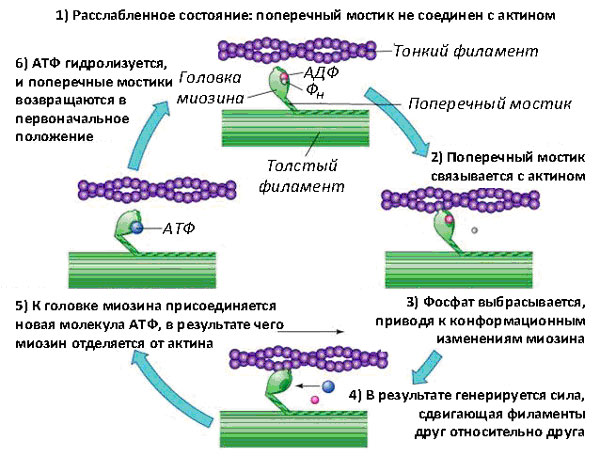
И вот начинается кое-что интересное. Импульс, подошедший к нервно-мышечному соединению, вызывает повышение внутриклеточного уровня кальция. Кальций присоединяется к регуляторным белкам, которые обматывали актин и загораживали его от миозина, в результате чего эти белки смещаются, и головка миозина, содержащая продукты гидролиза АТФ, приникает к молекуле актина. В результате различных пертурбаций (которые подробно описаны ниже), миозин крепко сцепляется с актином и меняет свою конформацию, поворачивая хвост относительно головки и выплевывая продукты гидролиза. Это происходит на множестве миозиновых головок и приводит к тому, что актиновая нить чуть-чуть сдвигается относительно миозиновой. Затем крепко сцепленный с актиновой нитью миозин связывается с АТФ, отцепляется от актина и претерпевает обратные конформационные изменения — то есть отворачивает хвост обратно (рис. 3).
Так, перебирая головками, миозиновые молекулы и обеспечивают работу мышцы. Расслабление же мышц происходит тогда, когда к мышечной клетке перестал подходить импульс и в нее перестал поступать кальций. Тогда отцепившиеся друг от друга актиновые и миозиновые нити постепенно возвращаются в свое первоначальное положение (отчасти благодаря эластичным свойствам молекул титина), и мышца расслабляется.
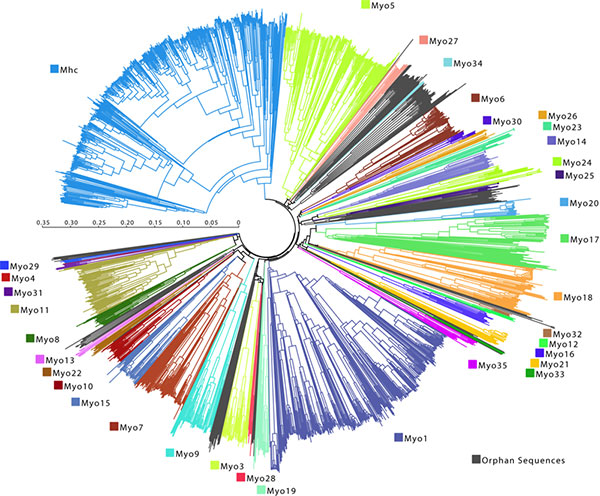
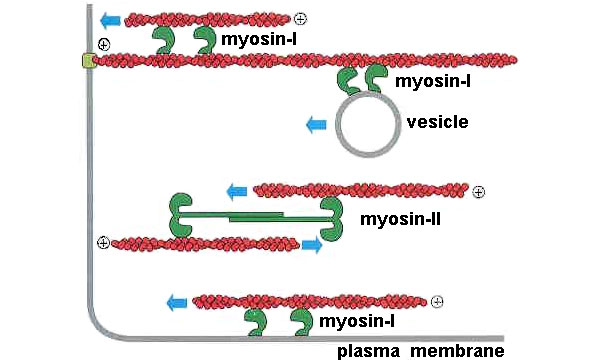
Вообще, способность миозина двигаться вдоль актиновой нити — это слишком удобное свойство, чтобы использовать его только для мышечного сокращения. Поэтому множество различных видов миозина (их еще называют «миозиновыми моторами», их филогенетическое дерево показано на рис. 4) применяется разными видами клеток для множества разнообразных функций — помимо собственно сокращения мышц они могут обеспечивать внутриклеточный транспорт, двигать трансмембранные белки и так далее (рис. 5).
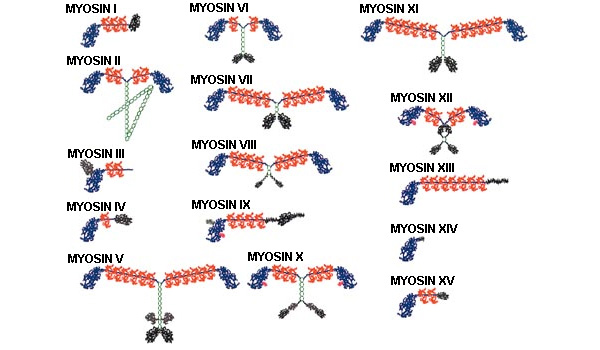
Различные миозины сильно отличаются друг от друга по строению (рис. 6): они могут быть одноголовыми или двухголовыми, с длинными или короткими хвостами; однако главная функциональная часть — головка — имеет практически одинаковое строение у всех видов миозина. То есть принцип работы миозина одинаков во всех случаях, а детали (например, размер хвоста) обеспечивают ту или иную специализацию.
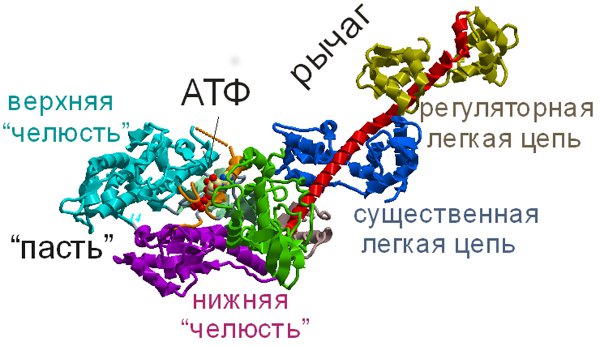
Миозины — это не единственные моторные белки. Помимо них существует еще два класса моторов — динеины и кинезины. В отличие от миозинов, которые двигаются по актиновой нити, динеины и кинезины бегают по микротрубочкам, причем динеины — только в одну сторону, а кинезины — только в противоположную. Гипотеза рычагаТеперь пришло время подробней разобраться, что же происходит с миозином при мышечном сокращении. Начнем с общепринятой в настоящее время теории, известной под названием «Гипотеза рычага». Посмотрим внимательнее на молекулу миозина (а конкретнее — самого удобного для исследований миозина II, рис. 7). Понятно, что в головке миозина должно быть как минимум два важных места — одно, хватающееся за актин, и второе, в которое залезает АТФ. Исследователи, работающие с миозином, остроумно назвали «актиновый» участок головки «пастью», а «АТФный» — «карманом». И пертурбации, происходящие с миозином, можно описать довольно грубым выражением: «закрой пасть и держи карман шире».
Дело в том, что, чтобы АТФный карман открылся и в него мог попасть АТФ, актиновая пасть должна быть закрыта (то есть миозин должен сидеть на актине): закрытая верхняя челюсть пасти оттягивает створку кармана, и тот открывается. АТФ влезает в широко раскрытый карман. И вот тут начинается самое интересное. Гидролиз АТФ может происходить только в закрытом кармане, а для того, чтобы карман закрылся, должна открыться пасть — то есть миозин должен отвалиться от актина. Но это еще не всё. Чтобы обеспечить гидролиз, окрестности кармана должны немного перестроиться, сдвинуться. Сдвигаясь, околокарманные участки вызывают небольшие изменения соседних областей, которые, в свою очередь, приводят к тому, что жесткий домен миозина под названием «конвертер» перебрасывается из одного устойчивого положения в другое и тянет за собой миозиновый хвост, отклоняя его на целых 60°. Курок взводится. Теперь начинается следующий акт. Миозин с карманом, набитым АДФ и фосфатом, должен обязательно прильнуть к актину и закрыть пасть, потому что иначе выплюнуть фосфат он не в состоянии (то есть чисто теоретически он его когда-нибудь выплюнет, но очень нескоро; поэтому миозин — это, по сути, актин-зависимая АТФаза). Миозин сначала слабо связывается с актином при помощи электростатических взаимодействий, а затем запускается процесс закрытия пасти. Происходит это так. В результате конформационных изменений миозиновая головка разворачивается к актиновой нити таким образом, что, во-первых, образует контакт, очень большой по площади (больше 18 нм2!), а во-вторых, миозин сцепляется сразу с двумя актиновыми молекулами с помощью гидрофобных и электростатических взаимодействий, в результате чего сродство миозина к актину оказывается в тысячу раз выше, чем при первом соединении. Итак, миозин выплевывает фосфат и, крепко-накрепко вцепившись в актин, претерпевает обратные конформационные изменения — хвост его «выстреливает», сдвигается относительно головки. Это происходит сразу на множестве молекул миозина и потому приводит к движению актиновой нити относительно миозиновой, а следовательно — и к сокращению мышцы. После этого АДФ выбрасывается из кармана. Миозин остается сцеплен с актином; пасть его закрыта — даже заперта! — крепко-накрепко, и если клетка мертва и все АТФ в ней уже закончились, то на этом грустном моменте история заканчивается, миозин и актин так и остаются в навсегда сцепившемся, застывшем состоянии, а у организма начинается трупное окоченение. Более оптимистичный сценарий, характерный для живой клетки с солидным запасом АТФ, предполагает, что в карман (который, как мы помним, головка с закрытой пастью держит шире) влезает новая молекула АТФ, пасть открывается, миозин отлипает от актина и цикл повторяется заново. Roll and lock: поворачиваем и запираемПо гипотезе рычага, в мышечном сокращении существует только один момент генерации силы — когда поворачивается миозиновый хвост (рычаг). Однако некоторые данные рентгенографии и томографии мышц не то чтобы не согласуются с этой теорией, а свидетельствуют о том, что существует еще какой-то непонятный момент в сокращении мышцы, который гипотеза рычага не объясняет. Поэтому группа исследователей под руководством А. К. Цатуряна предложила теорию мышечного сокращения под названием «Roll and lock» — «Поворачиваем и запираем» (см.: Michael A. Ferenczi et al., 2005. The «Roll and Lock» Mechanism of Force Generation in Muscle). По этой теории, миозиновые головки садятся на актин еще до гидролиза АТФ, причем садятся не стройно и организованно, а как попало. На головке миозина есть длинный выступающий домен — «щуп», — который «нащупывает» подходящую себе (кислую и отрицательно заряженную) часть актиновой нити и прилипает к ней — как придется, под первым попавшимся углом. Однако стоит произойти гидролизу АТФ, как миозин меняет свою конформацию, головки поворачиваются под нужным углом и крепко и четко, как ключ с замком, сцепляются с актиновой нитью, а из миозинового кармана выбрасывается фосфат. И вот только после этого происходит поворот рычага. Иными словами, модель получается двухстадийной — на первом этапе головка миозина крепко и четко вцепляется в актин и при этом немного поворачивается, а на втором — поворачивается рычаг, причем сила, которая потом приведет к движению мышцы, генерируется на обоих этих этапах. Помимо рентгеноструктурных и томографических данных, которые очень хорошо согласуются с теорией «Roll and lock», существует и несколько косвенных, но очень красивых доказательств ее правоты. Например, известно, что во время мышечного сокращения, в том случае, если мышца не меняет свою длину, всего чуть более 40% миозиновых головок сидит на актине, а остальные болтаются ни к чему не присоединенными. Однако когда сжатую мышцу насильно растягивают (например, такое бывает при беге, когда человек приземляется на напряженную мышцу), то жесткость мышцы резко увеличивается из-за того, что почти все свободные миозиновые головки резко сцепляются с актиновой нитью. Однако, судя по рентгеноструктурным данным, сцепляются они отнюдь не «намертво», как ключ с замком, а просто как попало. Объяснить это можно как раз с помощью теории «Roll and lock». Гидролиз АТФ при растяжении мышцы прекращается (оно и понятно: какой смысл тратить АТФ, если работа совершается не мышцей, а над мышцей), и все миозиновые головки переходят в состояние «активного актинового поиска» — их торчащий щуп ищет актиновую нить, нащупывает на ней подходящее место и сцепляется с ним — не крепко-накрепко, не как ключ с замком, а как попало. Однако для того, чтобы увеличить жесткость мышцы (и этим защитить кости от перелома) этого оказывается достаточно. ИтогГипотеза «Roll and lock» уточняет гипотезу рычага. Она лучше согласуется с экспериментальными данными и описывает мышечное сокращение более подробно. Но совершенно точно можно сказать, что и эта теория может быть уточнена и расширена — однако каким именно образом, мы пока еще не знаем. Мышечное сокращение, которое интенсивно и кропотливо исследуется уже многие годы, во многом по-прежнему остается неразгаданной загадкой. Видеоиллюстрации:
Источники:1) Лекции А. К. Цатуряна и С. Ю. Бершицкого на Зимней школе FutureBiotech. Вера Башмакова
ТегиПохожее
|
| Главная ≫ Инфотека ≫ Биология ≫ Как и почему мышцы сокращаются? Новая модель мышечного сокращения «Поворот и замок» |
|
[time: 11 ms; queries: 8]
22 Мая 2026 23:38:59 GMT+3 |


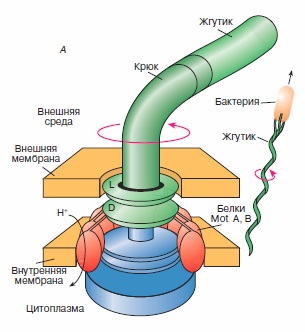 Рассмотрены строение и механизмы действия протонной АТРсинтазы и флагеллярного мотора - молекулярных моторов живой клетки, выполняющих химическую и механическую работу, связанную с их вращательным движением, строение и механизмы работы миозина и кинезина - механохимических белков, ответственных за сократительную активность и внутриклеточный транспорт органелл в клетке.
Рассмотрены строение и механизмы действия протонной АТРсинтазы и флагеллярного мотора - молекулярных моторов живой клетки, выполняющих химическую и механическую работу, связанную с их вращательным движением, строение и механизмы работы миозина и кинезина - механохимических белков, ответственных за сократительную активность и внутриклеточный транспорт органелл в клетке.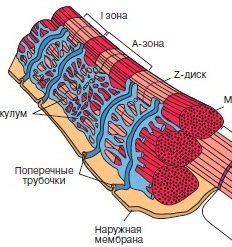 В основе сокращения мышц лежит взаимное перемещение двух систем нитей, образованных актином и миозином. АТФ гидролизуется в активном центре, расположенном в головках миозина. Гидролиз сопровождается изменением ориентации головок миозина и перемещением нитей актина. Регуляция сокращения обеспечивается специальными Са-связывающими белками, расположенными на нитях актина или миозина.
В основе сокращения мышц лежит взаимное перемещение двух систем нитей, образованных актином и миозином. АТФ гидролизуется в активном центре, расположенном в головках миозина. Гидролиз сопровождается изменением ориентации головок миозина и перемещением нитей актина. Регуляция сокращения обеспечивается специальными Са-связывающими белками, расположенными на нитях актина или миозина. Запах корицы и яблок — бабушкин пирог, запах хвои и мандаринов — Новый год, сладкий дурман черемухи — весна… Каждый человек сможет добавить к этому списку длинный ряд своих собственных ассоциаций. Многообразие растительных ароматов, созданных природой, кажется неисчерпаемым, многие из них абсолютно уникальны. Для обозначения таких веществ, которые не принимают непосредственного участия в росте, развитии и репродукции отдельных клеток, более 200 лет назад был предложен термин «вторичные метаболиты». Несмотря на несколько неуважительное название, вещества эти выполняют важную роль в жизни растения в целом, участвуют во взаимодействии растений друг с другом и с окружающей средой. К настоящему моменту идентифицировано более 100000 таких веществ, многие из которых являются легколетучими, и люди воспринимают их как запах растения. В этой лекции я постараюсь рассказать о некоторых особенностях пахучих растений, немного о том, как изучают биосинтез летучих вторичных метаболитов, а также о перспективах применения этих знаний на практике…
Запах корицы и яблок — бабушкин пирог, запах хвои и мандаринов — Новый год, сладкий дурман черемухи — весна… Каждый человек сможет добавить к этому списку длинный ряд своих собственных ассоциаций. Многообразие растительных ароматов, созданных природой, кажется неисчерпаемым, многие из них абсолютно уникальны. Для обозначения таких веществ, которые не принимают непосредственного участия в росте, развитии и репродукции отдельных клеток, более 200 лет назад был предложен термин «вторичные метаболиты». Несмотря на несколько неуважительное название, вещества эти выполняют важную роль в жизни растения в целом, участвуют во взаимодействии растений друг с другом и с окружающей средой. К настоящему моменту идентифицировано более 100000 таких веществ, многие из которых являются легколетучими, и люди воспринимают их как запах растения. В этой лекции я постараюсь рассказать о некоторых особенностях пахучих растений, немного о том, как изучают биосинтез летучих вторичных метаболитов, а также о перспективах применения этих знаний на практике… В научных представлениях о происхождении жизни в последнее десятилетие происходит настоящая революция, и она далеко не завершена. К сожалению, эта информация доступна в основном только на английском языке. Цикл статей, предлагаемый вниманию читателей, отчасти восполнит этот пробел.
В научных представлениях о происхождении жизни в последнее десятилетие происходит настоящая революция, и она далеко не завершена. К сожалению, эта информация доступна в основном только на английском языке. Цикл статей, предлагаемый вниманию читателей, отчасти восполнит этот пробел. Химики показали, что в гидротермальных источниках при температуре свыше 80 градусов может происходить абиогенный синтез органических веществ, в частности аминокислот, из угарного газа, цианистого водорода и других неорганических соединений. Это открытие — важный аргумент в пользу гипотезы, согласно которой жизнь на Земле зародилась в горячих вулканических источниках.
Химики показали, что в гидротермальных источниках при температуре свыше 80 градусов может происходить абиогенный синтез органических веществ, в частности аминокислот, из угарного газа, цианистого водорода и других неорганических соединений. Это открытие — важный аргумент в пользу гипотезы, согласно которой жизнь на Земле зародилась в горячих вулканических источниках. Какого цвета могут быть внеземные растения? С научной точки зрения это отнюдь не праздный вопрос, так как цвет поверхности планеты может указать нам, есть ли на ней жизнь, а точнее — живые организмы, усваивающие энергию света своей звезды путем фотосинтеза.
Какого цвета могут быть внеземные растения? С научной точки зрения это отнюдь не праздный вопрос, так как цвет поверхности планеты может указать нам, есть ли на ней жизнь, а точнее — живые организмы, усваивающие энергию света своей звезды путем фотосинтеза. Эта книга предназначена для широкого круга читателей, желающих узнать больше об окружающем нас мире и о самих себе. Автор, известный ученый и популяризатор науки, с необычайной ясностью и глубиной объясняет устройство Вселенной, тайны квантового мира и генетики, эволюцию жизни и показывает важность математики для познания всей природы и человеческого разума в частности.
Эта книга предназначена для широкого круга читателей, желающих узнать больше об окружающем нас мире и о самих себе. Автор, известный ученый и популяризатор науки, с необычайной ясностью и глубиной объясняет устройство Вселенной, тайны квантового мира и генетики, эволюцию жизни и показывает важность математики для познания всей природы и человеческого разума в частности. Самый редкий элемент в земной коре, самым тяжелый газ, самый тугоплавкий материал, самый сильный стабильный окислитель, самая сильная кислота, самый сильный яд, самое сладкое вещество — и другие рекорды.
Самый редкий элемент в земной коре, самым тяжелый газ, самый тугоплавкий материал, самый сильный стабильный окислитель, самая сильная кислота, самый сильный яд, самое сладкое вещество — и другие рекорды.